Energia di ionizzazione
Cos'è l'energia di ionizzazione
L'energia di ionizzazione è l'energia necessaria per togliere un elettrone da un atomo isolato allo stato gassoso.
Si chiama energia di ionizzazione perché la fuoriuscita di un elettrone trasforma un atomo neutro in uno ione positivo (catione).
$$ X(g) \rightarrow X^+(g) + e^- $$
Esempio
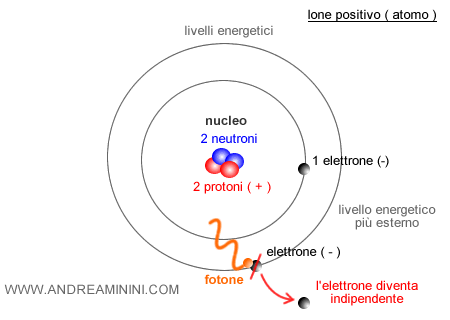
Nota. Per fuoriuscita di un elettrone si intende l'allontanamento di uno degli elettroni più esterni dell'atomo a una distanza infinita. Si parla di distanza infinita perché in tale caso non c'è sicuramente nessun'altra interazione tra l'atomo e l'elettrone.
Posso definire l'energia di ionizzazione anche come l'energia che lega un elettrone all'atomo.
Pertanto, quanto più alta è l'energia di ionizzazione di un atomo isolato, tanto più l'atomo ha una struttura elettronica stabile.
Ogni elemento chimico ha una propria energia di ionizzazione.
Come misurare l'energia di ionizzazione. L'energia di ionizzazione si misura in kJ prendendo come riferimento una mole di atomi. $$ \frac{kJ}{mol} $$ o in modo equivalente $$ kJ \cdot mol^{-1} $$
L'energia di prima e seconda ionizzazione
L'energia di ionizzazione si distingue in prima e seconda ionizzazione.
- L'energia di prima ionizzazione
E' l'energia necessaria per far uscire il primo elettrone da un atomo neutro. - L'energia di seconda ionizzazione
E' l'energia necessaria per far uscire il secondo elettrone dall' atomo.
E ovviamente si parla di energia di terza, quarta, quinta ionizzazione per i successivi.
L'energia di seconda ionizzazione è sempre più alta dell'energia di prima ionizzazione perché il secondo elettrone viene rimosso da uno ione positivo invece che da un atomo neutro.
Lo ione positivo ha una carica nucleare per elettrone più alta, quindi un legame e una forza di attrazione maggiore sugli elettroni.
Nota. In particolar modo, l'energia di seconda ionizzazione è molto elevata se lo ione ha una struttura elettronica stabile (es. i metalli alcalini del gruppo I A). E' meno marcata, invece, se la rimozione di due elettroni porta gli ioni ad avere una struttura molto stabile simile a quella dei gas nobili ( es. i metalli alcalino-terrosi del gruppo II A).
L'energia di ionizzazione negli elementi chimici
Gli elementi chimici hanno diversi livelli di energia di ionizzazione.
Questo accade perché il numero atomico (Z) ossia la quantità di protoni/elettroni influisce sul legame tra gli elettroni più esterni e il nucleo dell'atomo.
L'energia di ionizzazione aumenta progressivamente al crescere del numero atomico in uno stesso periodo.
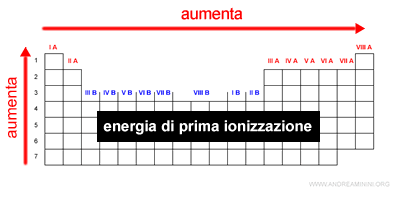
Sulla tavola periodica l'energia di ionizzazione cresce da sinistra verso destra.
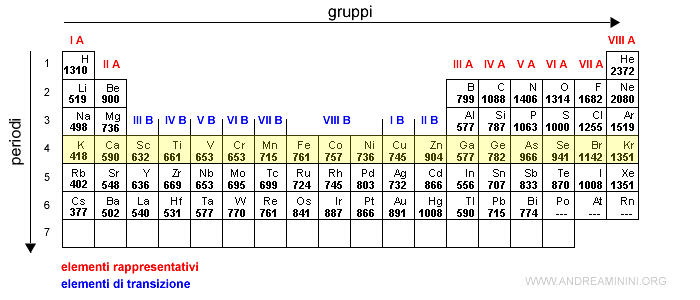
Il valore minimo dell'energia di ionizzazione in un periodi si riscontra nel primo gruppo I A ( metalli alcalini ) perché hanno un solo elettrone di valenza.
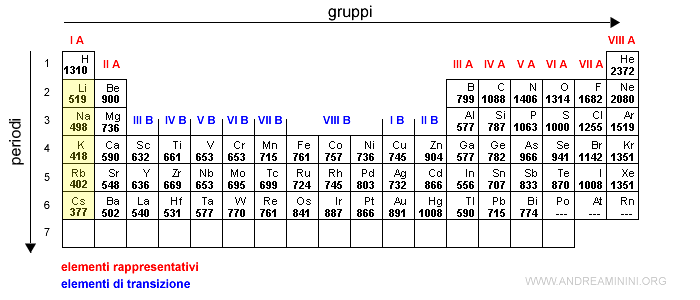
Nei metalli alcalini la carica nucleare per elettrone (forza attrattiva) è minore rispetto agli altri elementi dello stesso periodo.
Inoltre, i livelli intermedi pieni di elettroni si frappongono tra il nucleo e gli elettroni di valenza, riducendo l'interazione tra gli elettroni più esterni e il nucleo atomo.
Pertanto il legame è più debole e l'energia di ionizzazione è più bassa.
Esempio. La configurazione di un atomo di litio è 1s22s1. I due elettroni nell'orbitale 1s sono uno schermo tra il nucleo e l'elettrone di valenza nell'orbitale 2s. Quando si rimuove un elettrone da un metallo alcalino, l'elemento si trasforma in uno ione positivo con una struttura elettronica simile a quella dei gas nobili. Pertanto, gli ioni positivi dei metalli alcalini sono particolarmente stabili. Ad esempio, lo ione di litio Li+ ha una struttura elettronica simile all'elio (1s2).
Man mano che aumenta il numero atomico (Z) sullo stesso periodo, aumenta la forza di attrazione del nucleo perché aumenta la carica nucleare per elettrone a parità di volume atomico.
La carica nucleare rafforza il legame tra gli elettroni e il nucleo, ostacolando la fuoriuscita degli elettroni più esterni.
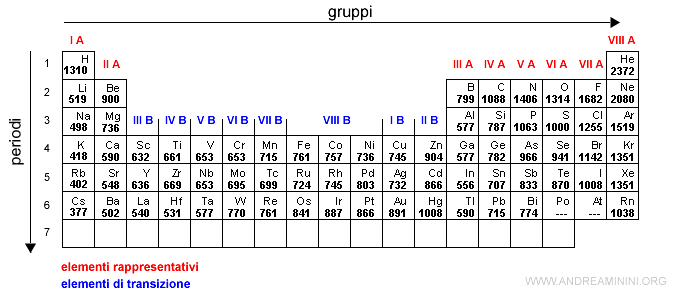
Tuttavia l'incremento dell'energia di ionizzazione in un periodo non è lineare.
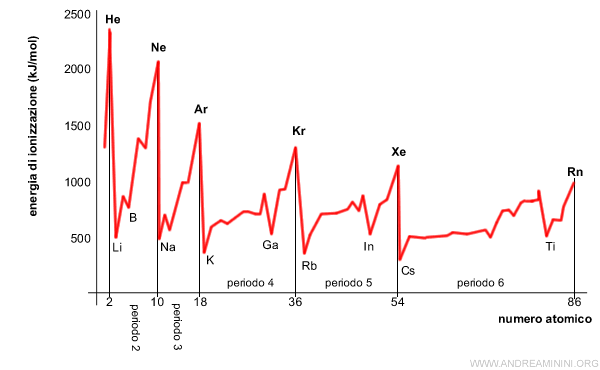
In alcuni casi, l'incremento del numero degli elettroni negli orbitali di tipo p aumenta la forza di repulsione tra gli elettroni a tal punto da compensare la maggiore forza di attrazione del nucleo.
Esempio. L'energia di ionizzazione dell'ossigeno (O) è più bassa dell'azoto (N) ma con il fluoro (F) torna a crescere.
Negli elementi di transizione l'energia di ionizzazione ha poche variazioni, è perlopiù costante, perché il raggio atomico non varia di molto.
Tuttavia, gli elementi di transizione non sono tutti uguali.
Alcune configurazioni elettroniche degli elementi di transizione sono molto più stabili di altre.
Esempio. Sono particolarmente stabili le configurazioni in cui gli elettroni si dispongono sugli orbitali di tipo d o f con lo stesso spin (d5 e f7). Nel caso della struttura d5 è occupata la metà dei posti disponibili negli orbitali di tipo d (10). Per il principio di Hund i primi elettroni si dispongono sul sottolivello con lo stesso spin. Lo stesso accade nel caso della struttura f7 perché è occupata la metà dei posti disponibili sugli orbitali di tipo f (14.
Negli elementi di transizione del sesto periodo si manifesta una particolarità.
Alcuni elementi di transizione hanno un'energia di ionizzazione superiore rispetto agli elementi dello stesso gruppo che si trovano nei periodi precedenti.
Questo accade perché 14 elementi delle terre rare (lantanidi) si dispongono sugli orbitali 4f prima degli orbitali 5d. Quindi, la carica nucleare è molto più forte.
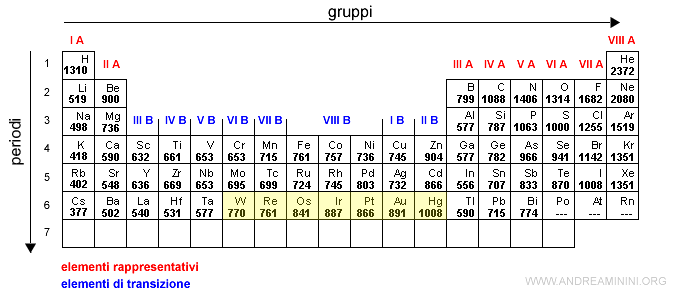
Nota. L'oro (Au) si trova sul sesto periodo e ha un'energia di ionizzazione pari a 891 kJ/mol. L'argento (Ag) si trova nello stesso gruppo dell'oro ma al quinto periodo e ha un'energia di ionizzazione più bassa, pari a 732 kJ/mol.
Il valore massimo di un periodo viene raggiunto con il gruppo dei gas nobili, in quanto hanno una struttura atomica particolarmente stabile da cui è molto più difficile rimuovere un elettrone.
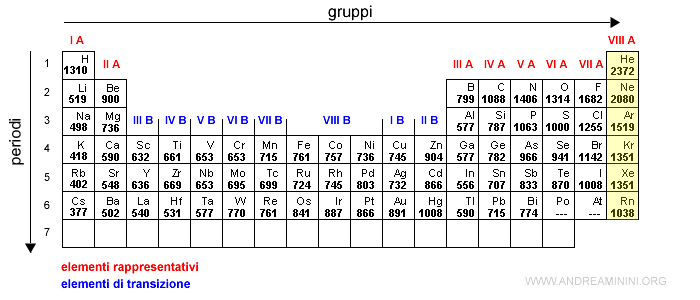
Quando si passa al periodo successivo, l'energia di ionizzazione crolla bruscamente perché gli ultimi elettroni si dispongono su un livello energetico più esterno (numero quantico principale).
Sul livello energetico più esterno la forza di attrazione del nucleo sugli elettroni più esterni è più bassa.
E così via
