La formula chimica
Cos'è una formula chimica
Una formula chimica rappresenta graficamente una molecola, indica quanti e quali atomi compongono una molecola.
Il significato della formula chimica cambia a seconda del composto chimico.
- Se nel composto chimico è individuabile una molecola, la formula chimica dice quanti e quali atomi compongono la molecola.
Esempio. L'acqua ha una molecola composta da due atomi idrogeno e un atomo di ossigeno (H2O).
- Se nel composto chimico non è individuabile una molecola, la formula chimica esprime soltanto il rapporto atomico tra gli atomi del composto chimico.
Esempio. Nel cloruro di sodio (NaCl) si può soltanto dire che il rapporto tra gli atomi è 1 a 1.
Come si scrive una formula chimica
Il simbolo di una formula chimica si ottiene scrivendo i simboli degli elementi chimici che la compongono.
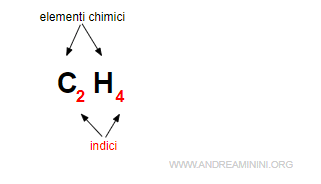
Ogni elemento chimico è accompagnato da un numero intero, detto indice, in pedice in basso a destra per indicare il numero di atomi dell'elemento nella molecola.
Se l'indice è uguale a uno, si omette.
Esempio. Una molecola d'acqua è composta da due atomi di idrogeno (H2) e un atomo di ossigeno (O). $$ H_2O $$ Il simbolo dell'idrogeno H ha in pedice il numero 2. Questo vuol dire che nella molecola ci sono due atomi di idrogeno. Poiché nella molecola d'acqua c'è un solo atomo di ossigeno, l'indice in pedice si omette e scrivo semplicemente O. Non si scrive O1.
Il coefficiente numerico prima della molecola, se presente, indica il numero delle molecole dello stesso tipo.
Il coefficiente si omette se è uguale a uno.
Esempio. Questa formula indica 3 molecole d'acqua $$ 3 H_2O $$ Per indicare una sola molecola d'acqua scrivo semplicemente H2O. Non si scrive 1H2O.
Una molecola può essere composta anche da due o più atomi dello stesso elemento chimico.
Non devono essere necessariamente elementi diversi.
Esempio. Questa formula indica una molecola di ossigeno composta da due atomi di ossigeno. $$ O_2 $$ E' importante sottolineare che la formula O2 è differente dalla formula 2O. La formula O2 indica due atomi di ossigeno legati tra loro in una molecola. La formula 2O, invece, indica due atomi di ossigeno allo stato atomico, ossia non legati tra loro in una molecola. Le proprietà fisiche e chimiche degli atomi sono diverse quando si trovano in una molecola.
Se è necessario indicare lo stato fisico della materia, si può aggiungere in pedice a destra dell'elemento o del composto il simbolo dello stato fisico tra parentesi tonde:
- (s)=solido
- (g)=aeriforme
- (l)= liquido.
Esempio. La molecola d'acqua può trovarsi allo stato liquido, solido o aeriforme. $$ H_2O _{(l)} = \text{acqua allo stato liquido} $$ $$ H_2O _{(s)} = \text{acqua allo stato solido (ghiaccio) } $$ $$ H_2O _{(g)} = \text{acqua allo stato aeriforme (vapore acqueo) } $$
Tipi di formule
Esistono tre tipi di formule
- La formula minima (o empirica)
La formula minima indica il rapporto di combinazione atomica. E' detta minima (o empirica) perché riporta il rapporto tra atomi diversi e non il reale numero degli atomi.Esempio. La formula minima dell'etano è CH3 perché in una molecola di etano per ogni atomo di carbonio ci sono tre atomi di idrogeno. $$ CH_3 $$
Nella formula minima il rapporto tra gli atomi degli elementi chimici diversi deve essere composto da coefficienti interi e minimi.Esempio. Non è corretto scrivere H4O2, né HO0.5 come formula minima. E' invece corretto scrivere H2O.
- La formula molecolare
La formula molecolare indica il reale numero di atomi dei diversi elementi chimici presenti in una molecola. La formula molecolare può essere coincidente oppure multipla della formula minima per un numero intero.Esempio. La formula molecolare dell'etano è C2H6 perché una molecola di etano è composta da due atomi di carbonio e sei atomi di idrogeno. $$ C_2 H_6 $$ In questo caso la formula molecolare (C2H6) è multipla della formula minima (CH3) per un fattore pari a due.
- La formula di struttura
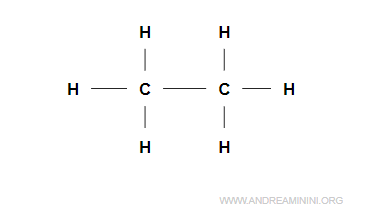
La formula di struttura rappresenta quali e quanti atomi sono presenti in una molecola e come sono legati gli atomi. In pratica, indica anche i legami tra gli atomi, ossia la posizione di ogni atomi nella struttura della molecola. I legami sono rappresentati da linee che collegano i simboli degli atomi.Esempio. La formula di struttura dell'etano si presenta in questo modo. Oltre alla quantità e qualità degli atomi, sono presenti anche i legami tra gli atomi della molecola di etano.
La formula di struttura è indispensabile per studiare i composti del carbonio perché cambiando la posizione di un atomo cambia il carattere del composto.