Come bilanciare la massa di un'equazione chimica
Per bilanciare la massa di un'equazione chimica
- Conto gli atomi di un elemento chimico a sinistra e a destra
- Se il numero di atomi non è lo stesso, modifico i coefficienti stechiometrici per eguagliarlo
- Ripeto le stesse operazioni per ogni elemento dell'equazione chimica
Un esempio
Provo a bilanciare questa equazione chimica
$$ BaCl_2 + Fe_2(SO_4)_3 \rightarrow BaSO_4 + FeCl_3 $$
Non è una reazione redox perché gli elementi mantengono lo stesso numero di ossidazione sia nei reagenti che nel prodotto.
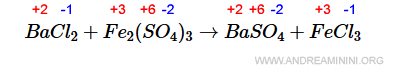
In genere è sempre meglio cominciare da un metallo o un non metallo.
Solo in casi rari si inizia dall'ossigeno o dall'idrogeno.
Bario
Comincio dal bario (Ba) che ha un atomo a sinistra e un atomo a destra. Quindi, è bilanciato.
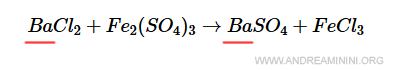
Cloro
Il cloro (Cl) ha 2 atomi a sinistra e 3 atomi a destra.
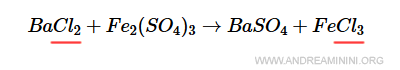
Per bilanciare moltiplico per 3 il termine a sinistra e per 2 il termine a destra, in questo modo ci sono 6 atomi di cloro sia a sinistra che a destra.
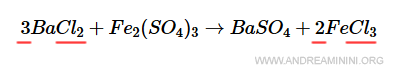
Poiché la modifica cambia anche il numero di atomi di bario, già analizzato, provvedo subito a ribilanciarlo.
Ci sono tre atomi di bario a sinistra e uno a destra.
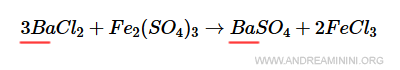
Quindi, moltiplico per tre il termine a destra.
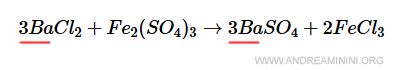
In questo modo ci sono 3 atomi di bario a destra e a sinistra.
Ferro
Passo ad analizzare il ferro (Fe). Ci sono due atomi di ferro a sinistra e 2 atomi di ferro a destra.
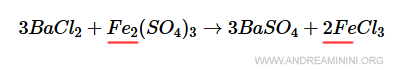
E' già bilanciato. Non devo fare nulla.
Zolfo
Lo zolfo (S) ha 3 atomi a sinistra e 3 atomi a destra.
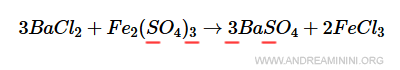
E' già bilanciato. Non devo fare nulla.
Ossigeno
Una volta bilanciati i metalli e i non metalli, analizzo l'ossigeno. L'ossigeno (O) ha 12 atomi a sinistra e 12 atomi a destra.
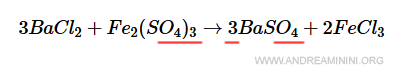
E' già bilanciato. Non devo fare nulla.
Il risultato finale
L'equazione è bilanciata perché tutti gli elementi chimici hanno lo stesso numero di atomi sia a sinistra che a destra.
$$ 3BaCl_2 + Fe_2(SO_4)_3 \rightarrow 3BaSO_4 + 2FeCl_3 $$
E così via.
