Dimensioni atomiche
Qual è la dimensione dell'atomo
La dimensione di un atomo (volume atomico) dipende dalla nube elettronica che circonda il nucleo. Il volume atomico è pari al rapporto tra il peso atomico e la densità dell'atomo. $$ \text{volume atomico} = \frac{\text{peso atomico}}{\text{densità dell'atomo}} $$
Quando si parla di dimensioni di un atomo non si considera soltanto il nucleo atomico ma anche le particelle che vi orbitano intorno ossia gli elettroni.

Considerando anche le orbite l'atomo occupa uno spazio almeno 10mila volte superiore e in gran parte è composto dallo spazio vuoto.
L'insieme degli orbitali dove si trovano gli elettroni formano una nube elettronica intorno all'atomo.
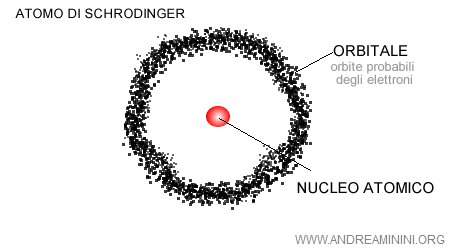
Il volume della nube elettronica varia a seconda degli elementi chimici, perché un atomo stabile può avere uno o più elettroni.
In un atomo neutro il numero degli elettroni eguaglia il numero dei protoni ( numero atomico ).
Quanti più elettroni orbitano intorno al nucleo atomico, tanto più ampia è la nube elettronica dell'atomo perché gli ultimi elettroni tendono a spostarsi sugli orbitali più energetici e più distanti dal nucleo.
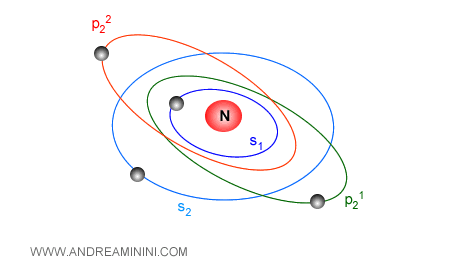
Pertanto, il raggio di un atomo è molto variabile negli elementi chimici.
Esempio. E' molto corto nell'idrogeno perché ha un solo elettrone (Z=1), è molto ampio nell'uranio perché ci sono novantadue elettroni (Z=92).
L'esperimento di Meyer
Nel 1870 il chimico L.Meyer studiò le variazioni del volume atomico negli elementi chimici.

Il volume atomico cresce tendenzialmente al crescere del numero atomico ma presenta uno schema regolare non strettamente crescente.
Nei metalli alcalini (gruppo IA della tavola periodica senza l'idrogeno) il volume atomico è più alto, mentre negli elementi centrali dei periodi tende a ridursi.
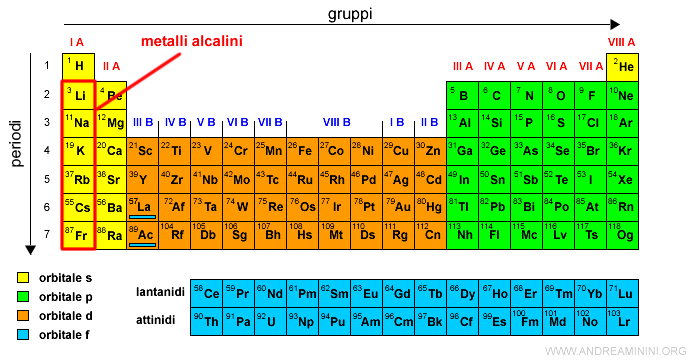
Nota. Osservando il grafico precedente dell'esperimento di Meyer, si nota subito che il volume atomico ha dei massimi locali con il numero atomico (Z) dei metalli alcalini Li, Na, K, Rb, Cs.
E così via.
