Idrossidi
Cosa sono gli idrossidi
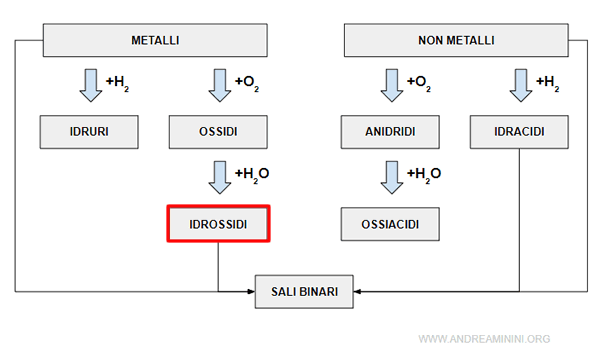
Gli idrossidi sono composti ternari formati da un metallo, l'ossigeno e l'idrogeno. Si formano per reazione tra gli ossidi basici e l'acqua.
Nella formula chimica di un idrossido si scrive prima il metallo, poi l'ossigeno e infine l'idrogeno.
$$ Metallo (OH)_n $$
L'ossigeno e l'idrogeno formano un gruppo (OH) detto ossidrile. Dove n è la valenza del metallo.
Nella nomenclatura IUPAC è detto
Idrossido di [metallo]
Nel caso ci siano più gruppi (OH), ossia n>1, si aggiungono i prefissi di-, tri-, ecc. al termine idrossido.
Gli idrossidi sono composti ionici perché il metallo è uno ione positivo mentre l'ossidrile OH è uno ione negativo.
Il numero di ossidazione dell'ossidrile OH è -1 perché all'ossigeno (O) manca un elettrone per completare l'ottetto.
Spiegazione. La configurazione superficiale dell'idrogeno è 1s1 mentre quella dell'ossigeno è 2s2 2p4. L'idrogeno e l'ossigeno si legano in modo covalente mettendo in comune un elettrone. L'idrogeno raggiunge il duetto. Essendoci un solo atomo di idrogeno all'ossigeno manca ancora un elettrone per completare l'ottetto.
Quindi, l'ossigeno attira un elettrone dal metallo diventando uno ione negativo.
Il metallo cede un elettrone diventando uno ione positivo.
Un esempio pratico
Esempio 1
L'idrossido di sodio (soda caustica) è un esempio di idrossido
$$ NaOH $$
Esempio 2
Un altro esempio è il didrossido di ferro
$$ Fe(OH)_2 $$
Esempio 3
Un altro esempio è il tridrossido di alluminio.
$$ Al(OH)_3 $$
Nota. Il n.o. dell'ossidrile OH è -1. In questo caso ci sono tre ossidrili. Quindi, il gruppo (OH)3 ha n.o.=-3. Da questo si deduce il n.o. dell'alluminio pari a +3.
La nomenclatura tradizionale degli idrossidi
Nella nomenclatura tradizionale il nome degli idrossidi cambia a seconda se si forma uno o più idrossidi.
- Se il composto forma un solo idrossido il nome è detto
Idrossido di [metallo]
- Se, invece, il composto forma più idrossidi si aggiungono i suffissi -oso e -ico alla radice del nome del metallo.
[metallo] + oso
[metallo] + ico
Un esempio pratico
Il ferro (metallo) reagisce con i gruppi (OH) formando due idrossidi:
- Il didrossido di ferro detto idrossido ferrico $$ Fe(OH)_2 $$
- Il tridrossido di ferro detto idrossido ferroso $$ Fe(OH)_3 $$
E così via.
