Affinità elettronica
Cos'è l'affinità elettronica
L'affinità elettronica misura la tendenza di un atomo neutro allo stato gassoso ad assumere elettroni dall'esterno.
Quando un atomo neutro acquista un elettrone diventa uno ione negativo, perché il numero degli elettroni è superiore a quello dei protoni.
$$ X(g) + e^- \rightarrow X^-(g) $$
L'unità di misura dell'affinità elettronica è il kJ/mol. Si misura in riferimento a una mole di atomi.
L'affinità elettronica può essere positiva o negativa.
- negativa
L'atomo tende ad assumere un elettrone. - positiva
L'atomo tende a ostacolare l'ingresso di un elettrone.
Quanto più l'affinità negativa è un numero molto inferiore a zero, tanto più l'atomo tende ad assumere un elettrone dall'esterno.
Una definizione alternativa
Poiché per rimuovere un elettrone occorre impiegare un energia ( energia di ionizzazione ), l'affinità elettronica posso definirla anche in questo modo alternativo
L'affinità elettronica è l'energia liberata dall'atomo quando acquista un nuovo elettrone in uno degli orbitali più esterni.
L'affinità elettronica negli elementi chimici
L'affinità elettronica in valore assoluto segue lo stesso andamento periodico dell'energia di ionizzazione.
In genere, l'affinità elettronica aumenta in valore assoluto lungo un periodo all'aumentare del numero atomico.
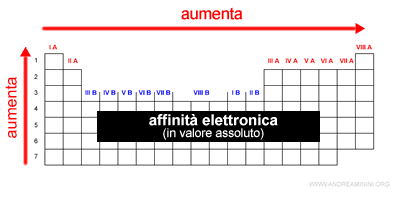
Muovendosi da sinistra verso destra su una riga della tavola periodica.
Ecco alcuni valori espressi in kJ/mol
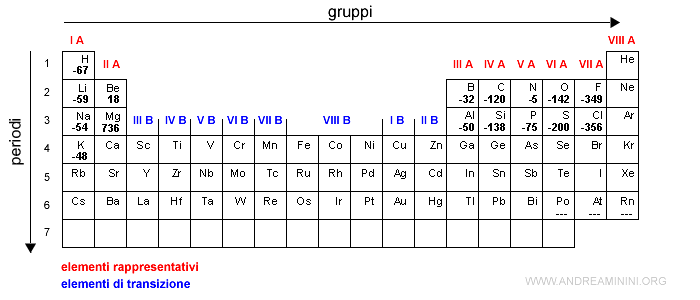
L'affinità elettronica è molto bassa nei gas nobili (ultimo gruppo) perché hanno lo strato più esterno completo e sono stabili.
E' invece molto alta negli alogeni perché con un solo elettrone in più gli atomi assumono una forma ionica stabile molto simile a quella dei gas nobili.
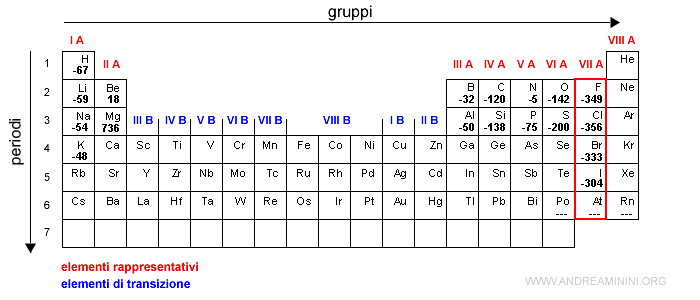
Esempio. La configurazione elettronica superficiale di un atomo di fluoro (F) è 2s22p5. Con l'acquisto di un elettrone la configurazione dello ione negativo F- diventa 2s22p6 pari a quella del neon (gas nobile).
L'affinità elettronica negli elementi di uno stesso gruppo si riduce con il periodo successivo.
Quindi, l'affinità elettronica cresce in valore assoluto se mi sposto sulla tavola periodica dal basso verso l'alto.

Le variazioni non sono comunque lineari perché si presentano diverse eccezioni.
E così via.
